DETECCIÓN IN VIVO DE ANGIOGÉNESIS PARA EL DIAGNÓSTICO TEMPRANO Y POSIBLE TRATAMIENTO DE NEOPLASIAS CON 99mTc-HYNIC-Arg-Gly-Asp Y 177Lu-DOTA- Arg-Gly-Asp POR TÉCNICAS DE MEDICINA NUCLEAR MOLECULAR (PRIMERA ETAPA)
Responsable: GUILLERMINA FERRO FLORES
Objetivos:
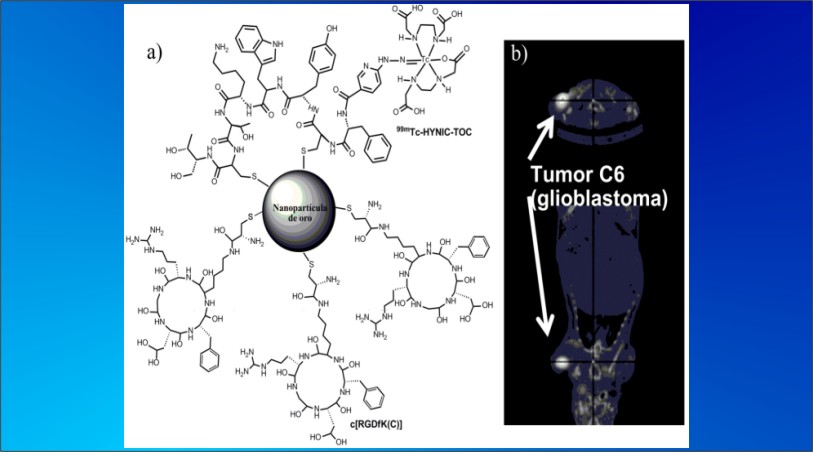
Preparar y evaluar sistemas multifuncionales de nanopartículas de oro radiomarcadas con 99mTc-HYNIC ó 177Lu-DOTA y conjugadas a la secuencia peptídica ciclo-Arg-Gly-Asp-D-Phe(Cys) [cRGDfK(C)] como agentes potenciales para la detección de angiogénesis in vivo en el diagnóstico temprano y posible tratamiento de cáncer de mama y glioblastomas. Asimismo realizar un estudio comparativo de la biocinética y captación tumoral in vivo de los sistemas multifuncionales 99mTc- ó 177Lu- AuNP-cRGDfK(C) con los sistemas monoméricos 99mTc-HYNIC-cRGDyK y 177Lu-DOTA-cRGDyK respectivamente.
Antecedentes:
La angiogénesis (formación de nuevos vasos sanguíneos) es un proceso crítico de los tumores para su crecimiento y diseminación (metástasis). Sin la producción de neovasculatura para proveer oxígeno y nutrientes, los tumores no pueden crecer más allá de 1-2 mm. El proceso angiogénico es regulado por receptores de adhesión celular tales como las integrinas α(v)β(3), las cuales funcionan como receptores para las proteínas de la matriz extracelular, reconociendo a todas ellas a través de la secuencia tri-peptídica arginina-glicina-ác. aspártico (Arg-Gly-Asp=RGD). La integrina α(v)β(3) está altamente expresada sobre la neovasculatura y en las células del tumor en el cáncer de mama y glioblastomas. La unión específica de las integrinas α(v)β(3) a la secuencia ciclo-RGD, es el fundamento para marcar al péptido c-RGD con radionúclidos para la obtención in vivo de imágenes de angiogénesis por técnicas de medicina nuclear molecular. La unión de decenas o centenas de péptidos a la superficie de una nanopartícula de oro (AuNP) podría producir un sistema multifuncional capaz de incrementar las uniones multivalentes de las NP-péptidos a sus receptores.
Diariamente se diagnostican en el país 25 casos de cáncer de mama, entre mujeres de 50 a 55 años. Desde 2006 el cáncer de mama es causante de un mayor número de muertes que el cáncer cérvicouterino. Los datos sobre detección estiman un incremento cercano a 16500 nuevos casos anuales para 2020. La mastografía es la técnica de elección en el diagnóstico de cáncer de mama y si bien los mamogramas adquiridos con equipo de rayos X detectan el 85 % de las lesiones en mama no son específicos y de hecho, solamente el 30% de esos pacientes, con biopsias ante la sospecha de cáncer, resultan ser positivos. Más aún, la mayoría de los casos se autodetecta y sólo 10% de todos los casos se identifica en etapa I. Los tumores gliales (glioblastomas) son las neoplasias primarias más frecuentes del sistema nervioso central (SNC) constituyendo cerca del 90 % en pacientes mayores de 20 años y presentando una supervivencia media de 12 meses. Estos tumores del SNC son la tercera causa de muerte en pacientes de 15 a 35 años y la segunda causa de muerte en menores de 15 años.
La expresión de la integrina α(v)β(3) correlaciona bien con la progresión e invasividad del tumor en cánceres de mama y glioblastomas. Asimismo, la sobre-expresión de las integrinas en eventos tempranos de la progresión del cáncer de mama ha quedado recientemente demostrado [Guo W. et al. Beta 4 integrin amplifies ErbB2 signaling to promote mammary tumorigenesis. Cell 126:489-502, 2006; Lahlou H. et al. Mammary epithelial-specific disruption of the focal adhesion kinase blocks mammary tumor progression. Proc Natl Acad Sci. USA 104:20302-20307, 2007; Pointer S.M., Muller W.J. Integrins in mammary-stem-cell biology and breast-cancer progression-a role in cancer stem cells?. Integrins in Stem cell and cancer initiation. J. Cell Sci. 122:207-214, 2009].
En este proyecto se propone preparar y evaluar sistemas multifuncionales de nanopartículas de oro radiomarcadas con 99mTc-HYNIC ó 177Lu-DOTA y conjugadas a la secuencia peptídica ciclo-Arg-Gly-Asp-D-Phe(Cys)[cRGDfK(C)] como agentes potenciales para la detección específica de angiogénesis in vivo en el diagnóstico temprano y posible tratamiento de cáncer de mama y glioblastomas. Asimismo realizar un estudio comparativo con los sistemas monoméricos 99mTc-HYNIC-cRGDyK y 177Lu-DOTA-cRGDyK. El proyecto está dividido en tres etapas:
ETAPA 1. PREPARACIÓN Y CARACTERIZACIÓN DE 4 CONJUGADOS DE RGD,
ETAPA 2. CARACTERIZACIÓN BIOQUÍMICA IN VITRO DE 4 CONJUGADOS DE RGD y
ETAPA 3. FARMACOCINÉTICA Y DOSIMETRÍA IN VIVO DE CONJUGADOS DE RGD.
Logros Obtenidos:
En concordancia con las metas propuestas para la primera etapa del proyecto, se obtuvieron y caracterizaron por técnicas espectroscópicas, radiocromatográficas y de microscopía, dos radiofármacos multivalentes y multiméricos de nanopartículas de oro conjugadas a péptidos derivados de RGD y marcadas con 99mTc ó 177Lu, así como dos radiofármacos que corresponden a sus respectivos monómeros: 99mTc-HYNIC-cRGDfK y 177Lu-DOTA-cRGDfK.
Publicaciones
ARTICULOS EN REVISTAS INTERNACIONALES
- Santos-Cuevas C.L., Ferro-Flores G.*, Rojas-Calderón E.L., García-Becerra R., Ordaz-Rosado D., Arteaga de Murphy C., Pedraza-López M. 99mTc-N2S2-Tat(49-57)-bombesin Internalized in Nuclei of Prostate and Breast Cancer Cells: Kinetics, Dosimetry and Effect on Cellular Proliferation. Nuclear Medicine Communications, 32(4) 303-313 (2011).
- Ferro-Flores G., Ocampo-García B.E., Meléndez-Alafort L. Development of Specific Radiopharmaceuticals for Infection Imaging by Targeting Infectious Micro-organisms. Current Pharmaceutical Design, , aceptado el 15 diciembre de 2011 (in press).
- Morales-Avila E., Ferro-Flores G., Ocampo-García B.E., De León L.M., Santos C.L., Medina L.A., Gómez L. Multimeric System of 99mTc-labeled Gold Nanoparticles Conjugated to c[RGDfK(C)] for Molecular Imaging of Tumor α(v)β(3) expression. Bioconjugate Chemistry 22(5) 913-922 (2011).
- Ocampo-García B.E., Ferro-Flores G., Morales-Avila E., Ramírez F. de M. Kit for Preparation of Multimeric Receptor-Specific 99mTc-Radiopharmaceuticals Based on Gold Nanoparticles. Nuclear Medicine Communications 32(11) 1095-1104 (2011).
- Ocampo-García B.E., Ramírez F. de M., Ferro-Flores G. De León L.M., Santos C.L., Morales E., Arteaga M.C., Pedraza M., Medina L.A., Camacho M.A. Technetium-99m labeled gold nanoparticles capped with HYNIC-peptide/mannose for sentinel lymph node detection. Nuclear Medicine and Biology, 38(1) 1-11 (2011).
- Jiménez-Mancilla N.P., Ferro-Flores G., Ocampo-García B.E., Luna-Guiterrez M.A., Ramírez F. de M., Pedraza-Lopez M., Torres-García E. Multifunctional targeted radiotherapy system for induced tumors expressing gastrin-releasing peptide receptors. Current Nanoscience, aceptado el 14 diciembre de 2011 (in press).
PRESENTACIONES EN CONGRESOS INTERNACIONALES:
- Morales-Avila E, Ferro-Flores G, Ocampo-Garcia B, De León-Rodriguez L, Santos-Cuevas CL, Medina L. 99mTc-labeled Gold Nanoparticles Conjugated to c[RGDfK(C)] for Molecular Imaging of Tumor αvβ3 Integrin Expression. 19th International Symposium on Radiopharmaceutical Sciences, Amsterdam, The Netherlands, August 28-September 2, 2011. Society of Radiopharmaceutical Sciences. J. Label. Compd. Radiopharm. 2011; 54:S534 (Abstract).
- Ocampo-Garcia B, Ferro-Flores G, Morales-Avila E, Ramirez F de M, Santos-Cuevas CL, Medina L. Kit for Instant Preparation of Multimeric Receptor-Specific 99mTc-Radiopharmaceuticals Based onf Gold Nanoparticles. 19th International Symposium on Radiopharmaceutical Sciences, Amsterdam, The Netherlands, August 28-September 2, 2011. Society of Radiopharmaceutical Sciences. J. Label. Compd. Radiopharm. 2011; 54:S535 (Abstract).
- Avila-Rodriguez MA, Ferro-Flores G, Pedraza-López M, Arteaga de Murphy C. Preparation and evaluation of 68Ga-DOTA-Glu-[cyclo(Arg-Gly-Asp-D-Phe-Lys)]2. 19th International Symposium on Radiopharmaceutical Sciences, Amsterdam, The Netherlands, August 28-September 2, 2011. Society of Radiopharmaceutical Sciences. J. Label. Compd. Radiopharm. 2011; 54:S353 (Abstract).
- Flores-Moreno A, Valle-González M, Zarate-Morales A, Ferro-Flores G, Pedraza-Lopez M, Arteaga de Murphy C, Avila-Rodriguez MA. Production of 68Ga for Preclinical by Irradiation of a Natural Zn Foil with 7 MeV Protons. 19th International Symposium on Radiopharmaceutical Sciences, Amsterdam, The Netherlands, August 28-September 2, 2011. Society of Radiopharmaceutical Sciences. J. label. Compd. Radiopharm. 2011; 54:S249 (Abstract).
CAPITULO EN LIBRO
Arteaga de Murphy C, Ferro Flores G, Vera Hermosillo H., Ocampo-García BE. RADIOFÁRMACOS. En 10ª edición de la Farmacopea de los Estados Unidos Mexicanos, Secretaría de Salud, Vol. 1 p. 1324-1365, 2011. ISBN-978-607-460-204-3.
MEMORIAS EN CONGRESOS NACIONALES:
Ferro Flores G., Arteaga de Murphy C., Pedraza-López M., Ocampo-García B., Garnica-Garza H., Pichardo-Romero P., Gutiérrez Z. Dosimetría y Microdosimetría de Radiofármacos para el Diagnóstico, Seguimiento y Posible Tratamiento de Tumores de Origen Neuroendócrino y Linfomas no Hodgkin. Segundo Encuentro Académico de Fondo Sectorial de Investigación en Salud y Seguridad Social SSA/IMSS/ISSSTE-CONACyT 2011. México D.F., 3-4 de noviembre, 2011. Memorias p. 50-52.
PRESENTACIONES EN CONGRESOS NACIONALES:
- Ferro Flores G. Radiofármacos: Base de la Imagen Molecular. Taller Internacional de Genética Humana. Del 18 al 19 de febrero de 2011. Toluca, Estado de México.
- Luna-Gutiérrez MA, Ferro-Flores G, Ocampo-García BE, Jiménez-Mancilla NP, Morales-Avila E, De León-Rodríguez L, Isaac-Olivé K. 177Lu-Labeled Monomeric, Dimeric and Multimeric RGD Peptides for the Therapy of αvβ3 Integrin-Positive Tumors. XII International Symposium, XXII National Congress on Solid State Dosimetry. 5 to 9 September 2011, Mexico City. Organizado por la Sociedad Mexicana de Irradiación y Dosimetría y la UAM-I.
- Jiménez-Mancilla NP, Ferro-Flores G, Ocampo-García BE, Luna-Gutiérrez MA, Ramírez F de M, Pedraza-López M, Torres-García E. Multifunctional targeted radiotherapy system for gastrin releasing peptide-receptor positive tumors. XII International Symposium, XXII National Congress on Solid State Dosimetry. 5 to 9 September 2011, Mexico City. Organizado por la Sociedad Mexicana de Irradiación y Dosimetría y la UAM-I.
INFORME TÉCNICO :
Ferro Flores G., Ocampo García BE, Ramírez de la Cruz F. de M., Arteaga de Murphy C. y Pedraza López M. DETECCIÓN IN VIVO DE ANGIOGÉNESIS PARA EL DIAGNÓSTICO TEMPRANO Y POSIBLE TRATAMIENTO DE NEOPLASIAS CON 99mTc-HYNIC-Arg-Gly-Asp Y 177Lu-DOTA-Arg-Gly-Asp POR TÉCNICAS DE MEDICINA NUCLEAR MOLECULAR (PRIMERA ETAPA). INFORME TÉCNICO ININ.GANS-2011-12-01 Diciembre, 2011, pp. 51.
TESIS DE DOCTORADO
Título: Efecto del péptido TAT(49-57) sobre la biocinética y dosimetría de radiofármacos análogos de la bombesina. Fecha de examen: 1 de Julio de 2011. Tesista: Clara Leticia Santos Cuevas. Doctorado en Ciencias con Especialidad en Física Médica. Facultad de Medicina, Universidad Autónoma del Estado de México. Tutor: Guillermina Ferro Flores y Leticia Rojas Calderón
TESIS DE MAESTRIA
TITULO: Estudio de las propiedades ópticas y dosimétricas del nanoconjugado 99mTc-EDDA/HYNIC-GGC-AuNP-Bombesina por efecto del tamaño de nanopartícula. FECHA DE EXAMEN: 16 de febrero, 2011. ALUMNO: Andrei N. Mendoza Sánchez. DIRECTOR: Guillermina Ferro Flores. MAESTRÍA EN CIENCIAS CON ES´PECIALIDAD EN FÍSICA MEDICA, Facultad de Medicina, Universidad Autónoma del Estado de México.
TESIS DE LICENCIATURA
ALUMNA: ANDREA VILCHIS JUÁREZ. TITULO: "Radiomarcado del péptido c-DOTA-RGD y c-DOTA-RGDf con Lu-177 y evaluación de su estabilidad in vitro e in vivo". FECHA DE EXAMEN: 10 de enero de 2011. ASESOR: Guillermina Ferro Flores. QUIMICA FARMACEUTICA BIOLOGA, Facultad de Química, UAEM
Aplicaciones:
Los radiofármacos obtenidos serán evaluados biológicamente in vitro e in vivo en una segunda y tercera etapa para definir cual ó cuales presentan las mejores características radiofarmacocinéticas para la detección específica de angiogénesis in vivo en el diagnóstico temprano y posible tratamiento de cáncer de mama y glioblastomas. Se realizará el registro sanitario correspondiente ante la Secretaría de Salud para su distribución a los diferentes centros de Medicina Nuclear en el País.
Vinculación:
Instituto Nacional de Ciencias Médicas y Nutrición Salvador Zubirán, Instituto Nacional de Cancerología, Universidad Autónoma del Estado de México.
31/03/2014 por Tonatiuh Rivero Gutiérrez
Proyectos 2011
Análisis de Seguridad de lo...
Aplicaciones de los plasmas...
Características y propiedad...
Comportamiento fisicoquímic...
Desarrollo de nanocatalizad...
Desarrollo de sistemas dosi...
DETECCIÓN IN VIVO DE ANGIOG...
Diseño de catalizadores uni...
Disminución de gases tóxico...
Dosimetría básica y aplicac...
Efecto de la radiación gamm...
Eliminación de CO2 y H2S me...
Estudio de los efectos de l...
Estudios astrofísicos, cosm...
Evaluación de la contaminac...
Evaluación de la reducción ...
EVALUACIÓN DEL EFECTO GENÉT...
Generación de armónicos rel...
Hidrofilicidad de polímeros...
Mejora en la confiabilidad ...
MODULACIÓN ENDÓGENA Y EXÓGE...
OXIDACIÓN DE TITANIO POR PL...
Preparación y caracterizaci...
Producción masiva de especi...
Producción y caracterizació...
Reacciones de baja energía ...
Reactores avanzados generac...
INSTITUTO NACIONAL DE INVESTIGACIONES NUCLEARES - ALGUNOS DERECHOS RESERVADOS © 2014 - POLÍTICAS DE PRIVACIDAD
Carretera México-Toluca s/n, La Marquesa Ocoyoacac, México
C.P. 52750 - Tel. +52(55) 53297200
Comentarios sobre este Sitio de Internet

